Estratto: Gli imballaggi attivi sono diventati oggetto di notevole attenzione, in particolare quelli a base di materiali biodegradabili, grazie alla loro capacità di migliorare la conservazione degli alimenti e prolungarne la durata di conservazione. Una base adatta per ottenere tali tipi di imballaggi si è rivelata essere costituita da polimeri di origine naturale, come l'idrossilpropilmetilcellulosa (HPMC) e la zeina. Pertanto, il presente studio si concentra sullo sviluppo di film utilizzando il metodo di colata a base di HPMC puro e miscele di HPMC e zeina. Sono stati sviluppati tre tipi di matrici polimeriche: film di HPMC puro, zeina HPMC 3:1 e zeina HPMC 1:1. Inoltre, tutti sono stati caricati con curcumina per migliorarne l'attività biologica, e principalmente quella antiossidante. Per studiare il potenziale di questi film, sono state stabilite alcune delle loro proprietà più importanti in termini di potenziale applicazione come materiale da imballaggio, come le proprietà meccaniche (deformazione a rottura, modulo di Young), le proprietà barriera (velocità di trasmissione del vapore acqueo) e la morfologia. Dopo l'aggiunta di zeina è stata riscontrata una variazione significativa del modulo di Young; è passato da 276,98 ± 28,48 MPa per HPMC puro a 52,17 ± 10,19 MPa in un rapporto 1:1 tra i polimeri. Nel frattempo, la deformazione a rottura ha mostrato un leggero calo dall'86,74 ± 8,64% al 72,44 ± 9,62%. Le proprietà barriera sono state influenzate anche dalla formazione del film composito e dall'aggiunta di polifenoli, riducendo la velocità di trasmissione del vapore acqueo da 913,07 ± 74,01 g/m² .24 h per HPMC puro a 873,05 ± 9,07 g/m² .24 h per il film in rapporto 1:1 e ulteriormente a 826,35 ± 33,67 g/m² .24 h dopo l'aggiunta di rutina a quest'ultimo. Un'ulteriore caratterizzazione della capacità di scavenger dei radicali liberi DPPH ha mostrato un andamento a forma di A simile ai valori del modulo di Young, dovuto alla presenza di legami idrogeno, che influenzano entrambe le proprietà delle strutture dei film. È stato condotto uno studio del comportamento termico e dello stato di fase dei film ottenuti mediante calorimetria differenziale a scansione prima e dopo l'aggiunta di polifenoli, indicando la completa transizione di fase della rutina dallo stato cristallino a quello amorfo.
(https://www.mdpi.com/2079-6412/16/1/669)
1. Introduzione
Il packaging attivo rappresenta un approccio moderno alla conservazione degli alimenti, migliorandone la qualità e prolungandone la durata di conservazione. La sua efficacia è dovuta all'interazione tra l'imballaggio e il prodotto o allo spazio di testa all'interno della confezione. Questi sistemi funzionano rilasciando composti attivi come antiossidanti o antimicrobici, oppure assorbendo sostanze nocive come ossigeno, etilene o umidità in eccesso, che contribuiscono a inibire la crescita microbica, ritardare l'ossidazione e mantenere le proprietà sensoriali [ 1 , 2 ]. Le tecnologie di packaging attivo includono scavenger di ossigeno, assorbitori di etilene per frutta e verdura, rivestimenti antimicrobici e film biodegradabili contenenti estratti naturali o oli essenziali. Soluzioni più avanzate prevedono sistemi a rilascio controllato e sensibili agli stimoli, che attivano il rilascio di sostanze protettive in condizioni specifiche come aumento dell'umidità, variazioni di temperatura o attività microbica, offrendo una conservazione più mirata ed efficiente [ 2 , 3 ]. Gli sviluppi recenti si concentrano su matrici biodegradabili e di origine biologica, come PLA, film proteici e materiali a base di polisaccaridi, combinati con composti antiossidanti o antimicrobici naturali. Questi materiali sono ecocompatibili e supportano la sostenibilità ambientale, migliorando attivamente la durata di conservazione degli alimenti. Studi sperimentali dimostrano che i film attivi biodegradabili possono ridurre la perdita di peso, sopprimere la crescita microbica e ritardare i processi ossidativi in frutta e verdura fresche tagliate. L'incorporazione di flavonoidi naturali come la rutina migliora ulteriormente le prestazioni antiossidanti e antimicrobiche di questi film, rendendoli candidati promettenti per soluzioni di imballaggio attive ecocompatibili [ 4 ]. L'idrossipropilmetilcellulosa (HPMC) è un derivato semisintetico della cellulosa ampiamente utilizzato in rivestimenti e imballaggi commestibili grazie alla sua eccellente capacità di formare film, trasparenza e lavorabilità [ 5 ]. Tuttavia, i suoi limiti, in particolare l'elevata sensibilità all'acqua, la plastificazione ad elevata umidità e la modesta resistenza meccanica, ne limitano l'uso più ampio nelle applicazioni di imballaggio [ 6 , 7 ]. Queste debolezze hanno motivato ampi sforzi per migliorare i film HPMC mediante miscelazione, reticolazione e incorporazione di riempitivi nano e microstrutturati. Infatti, diversi studi dimostrano che i film compositi HPMC rinforzati con nanocellulosa o polisaccaridi presentano una migliore resistenza alla trazione, una ridotta permeabilità ai gas e una migliore stabilità alle fluttuazioni di umidità [ 8 , 9 ]. La zeina, una proteina prolamina idrofobica del mais, è un altro materiale da imballaggio promettente. È caratterizzata da una bassa permeabilità all'ossigeno [ 10 ] e da buone proprietà filmogene [ 11 ]. Il suo carattere idrofobico intrinseco può migliorare il comportamento di barriera all'umidità e ai gas quando incorporato in miscele [ 12 ]. Tuttavia, i film di zeina sono fragili e richiedono plastificanti o partner di miscelazione per ottenere un'adeguata flessibilità meccanica [ 13 ]. La miscelazione di HPMC idrofilo con zeina idrofobica rappresenta quindi una strategia interessante per regolare la sensibilità all'acqua, le proprietà barriera e il comportamento meccanico dei film compositi risultanti. Recenti lavori sperimentali hanno dimostrato che la combinazione di HPMC e zeina ha prodotto film la cui morfologia, trasparenza e proprietà meccaniche erano regolate dalle interazioni polimero-polimero, dalla polarità del solvente e dalle condizioni di essiccazione. In particolare, l'uso di solventi misti acqua/etanolo ha promosso una separazione di fase controllata, creando distinte microstrutture HPMC-zeina che influenzano la resistenza alla trazione, l'allungamento e la resistenza all'umidità [ 14 ]. È stato inoltre dimostrato che fattori di lavorazione come il rapporto polimerico, il solvente di colata e il tipo di plastificante controllano la miscibilità del composito e le strutture delle microfasi [ 15 ]. Oltre alla modifica strutturale, c'è una crescente attenzione alla progettazione di film di imballaggio attivi che incorporano agenti antimicrobici e antiossidanti. Oli essenziali (EO), estratti vegetali e agenti antimicrobici e antiossidanti naturali possono prolungare la durata di conservazione degli alimenti, ma la loro volatilità e sensibilità richiedono strategie di incapsulamento per garantire stabilità e rilascio controllato. Nanoparticelle di zeina, nanocarrier lipofili ed emulsioni di Pickering sono emersi come vettori altamente efficaci per l'inclusione di oli essenziali all'interno di film polimerici idrofili [ 16 , 17 ]. I film a base di HPMC stabilizzati con nanocarrier hanno mostrato una migliore ritenzione dei composti attivi e prestazioni antimicrobiche migliorate [ 18 ]. Nonostante i promettenti progressi, permangono diverse sfide per l'aumento di scala dei film attivi HPMC-zeina, tra cui il controllo della morfologia di fase durante l'evaporazione del solvente, la garanzia della stabilità di conservazione degli agenti attivi incapsulati, il raggiungimento di prestazioni costanti in cicli di umidità e temperatura variabili e il rispetto degli standard normativi per i materiali a contatto con gli alimenti.
In questo studio, film compositi di HPMC e HPMC-zeina, caricati con curcumina per potenziarne l'attività antiossidante, sono stati preparati e caratterizzati in termini di proprietà strutturali, fisico-chimiche, meccaniche, termiche, barriera e antiossidanti. La novità di questo studio risiede nel collegamento diretto del rapporto HPMC-zeina alle interazioni mediate da legami idrogeno e alle prestazioni funzionali dei film attivi. Inoltre, lo studio chiarisce come la rutina immobilizzata nella matrice polimerica influenzi il comportamento del film. Collegando composizione, struttura e prestazioni, questo studio offre chiare linee guida per la progettazione di film attivi biodegradabili di HPMC-zeina destinati ad applicazioni di imballaggio alimentare.
2. Materiali e metodi
2.1 Materiali
L'idrossipropilmetilcellulosa (HPMC, Mw ≈ 80.103 g/mol), la zeina (Z, estratta dal mais, Mw = 20.103 g/mol, il poli(etilenglicole) (PEG, Mw = 400 g/mol), il 2,2-difenil-1-picril-idrazile (DPPH, Mw = 394,32 g/mol) e il triidrato di rutina (R, Mw = 664,57 g/mol) sono stati acquistati da Sigma Aldrich (Taufkirchen, Germania). Tutti i solventi sono stati utilizzati così come ottenuti, con un grado di purezza analitica, e non sono state apportate ulteriori modifiche.
2.2. Fabbricazione di pellicole
Per ottenere i film esaminati, è stato impiegato il metodo di fusione. In particolare, sono stati preparati 3 tipi di film polimerici: HPMC puro, HPMC 3:1 Z e HPMC 1:1 Z. A tale scopo, un totale di 1 g di materiale secco nei rapporti menzionati è stato sciolto in una miscela di etanolo/acqua in un rapporto 70/30 [ 19 ]. Questa soluzione è stata mantenuta a 70 °C per 1 ora e agitata a 1000 giri al minuto. Successivamente, è stata colata in una capsula di Petri ed essiccata a 60 °C per 1 ora e poi a 30 °C fino all'ottenimento di una struttura secca. Questo protocollo è stato mantenuto lo stesso per la preparazione di strutture caricate con rutina, ma la rutina è stata aggiunta insieme alla massa polimerica a una concentrazione di 3,8 mg/mL o pari a 2 mg/cm² di superficie del film. 2.3. Caratterizzazione del film
2.3.1. SEM
La morfologia superficiale dei campioni così preparati è stata visualizzata tramite microscopia elettronica a scansione (SEM). Film di dimensioni 2 × 2 cm sono stati posizionati su un supporto di alluminio, rivestiti con carbonio e oro da un evaporatore sotto vuoto Quorum Q150T Plus (Quorum Technologies, West Sussex, Regno Unito), e le immagini sono state acquisite tramite un rivelatore di elettroni a retrodiffusione (Prisma E SEM, Thermo Scientific, Waltham, MA, USA) a diversi ingrandimenti. Tutte le immagini sono mostrate con una barra di scala di 10 µm.
2.3.2. FTIR
Gli spettri infrarossi a trasformata di Fourier (FTIR) sono stati ottenuti utilizzando uno spettrofotometro Jasco FT/IR-4X (Jasco, Hachioji, Giappone). L'intervallo spettrale era 4000–400 cm −1 . Per ridurre al minimo il rumore di fondo dello strumento, con una risoluzione di 2 cm −1 , lo strumento ha scansionato ciascun campione 32 volte utilizzando un portafiltri specializzato. Il display mostra lo spettro FTIR medio.
2.3.3 Proprietà meccaniche
Per valutare il modulo di Young (YM) di tutti i campioni, insieme a sforzo e deformazione, è stato eseguito un test distruttivo. I film sono stati tagliati in strisce di dimensioni 10 × 40 mm e fissati con morsetti pneumatici sigillati in gomma con una distanza di 20 mm e deformati a una velocità di trazione di 1 mm/s. Per ogni tipo di campione, sono state eseguite almeno 10 ripetizioni. Il modulo di Young è stato calcolato sulla base della regione lineare delle curve sforzo-deformazione. I valori forniti sono medie con la relativa deviazione standard.
2.3.4. Proprietà barriera
La velocità di trasmissione del vapore acqueo delle strutture risultanti è stata valutata con un metodo gravimetrico. A tale scopo, è stato utilizzato uno strumento modello W3/031 (Labthink, Jinan, Cina). Il test è stato condotto nelle seguenti condizioni: una differenza di umidità costante dell'80% tra i due lati del film, una temperatura di 38 °C e un tempo di raccolta puntiforme di 60 minuti. Sono state eseguite tre ripetizioni per ciascun tipo di campione e i risultati presentati rappresentano la media di queste con deviazioni standard.
2.3.5. Proprietà superficiali e idrofilia
Le proprietà idrofobiche dei film compositi preparati sono state studiate in condizioni standard (temperatura ambiente e pressione atmosferica normale) utilizzando due liquidi diversi (acqua e diiodometano CH2I2 ) . Piccole goccioline da 2 μL di ciascuno dei liquidi sono state depositate con cura sulla superficie dei film utilizzando una microsiringa di precisione da 10 μL (Innovative Labor System GmbH, Ilmenau, Germania). Sulla superficie dei film sono state depositate 6 goccioline di ciascun liquido, dopodiché i risultati raccolti sono stati utilizzati per la determinazione delle proprietà idrofobiche di ciascun campione. Gli angoli di contatto sono stati determinati misurando l'angolo creato dalla tangente del profilo della goccia e dalla superficie dei film dalle immagini acquisite con una fotocamera ad alta risoluzione. Per l'analisi delle immagini acquisite è stato utilizzato il software ImageJ v1.51k, National Institutes of Health, Bethesda, MD, USA.
Seguendo l'equazione (teoria) di Owens e Wendt [ 20 ], l'energia libera superficiale di un solido, γ s , può essere espressa come somma dei contributi delle componenti γ s d e γ s p . Entrambe possono essere determinate dai dati dell'angolo di contatto di liquidi polari e non polari con dispersione nota, per le parti non polari, γ lv d , e polari, γ lv p , della loro energia interfacciale:dove θ è l'angolo di contatto e 𝛾𝑙 𝑣=𝛾𝑑𝑙 𝑣+𝛾𝑝𝑙 𝑣. 2.3.6. Stabilità termica e indagine sullo stato di fase
Il comportamento termico e lo stato di fase dei film polimerici prima e dopo l'aggiunta di rutina sono stati studiati utilizzando il metodo di calorimetria differenziale a scansione (DSC) con lo strumento Phoenix 204F1 (Netzsch Gerätebau GmbH, Selb, Germania). L'apparato è stato calibrato con uno standard di indio (Tm = 156,6 °C, ΔHm = 28,5 J/g) per quanto riguarda il flusso di calore e la temperatura. Circa 2-5 mg di ciascun tipo di campione sono stati inseriti in un contenitore di alluminio e sigillati prima della misurazione. L'intervallo di temperatura per questo studio è stato impostato tra 25 °C e 300 °C con un incremento di riscaldamento di 10 °C/min.
2.3.7. Attività antiossidante
Per valutare l'attività antiossidante, e quindi il potenziale di confezionamento attivo di queste strutture, è stata esaminata la loro capacità di scavenging nei confronti della soluzione di radicali liberi (DPPH). I film sono stati tagliati in 3 pezzi di dimensioni 1 × 1 cm e incubati in 2 mL di etanolo per 1 ora. Da queste soluzioni, sono stati prelevati 0,1 mL e aggiunti a 2,5 mL di soluzione etanolica di DPPH 0,1 mM. Questa miscela è stata incubata al buio per 45 minuti a temperatura ambiente e misurata a 517 nm utilizzando uno spettrofotometro (Metertech SP-8001; Metertech Inc., Nangang, Taipei, Taiwan). L'attività di scavenging è stata calcolata con la formula indicata:dove A 0 è l'assorbanza della soluzione DPPH all'ora iniziale e A 45 è l'assorbanza della soluzione DPPH all'ora finale dopo 45 min. 2.3.8. Analisi statistica
Per individuare le differenze significative tra i film con diversa composizione, i risultati sono stati analizzati mediante un test ANOVA bidirezionale utilizzando il software Statistica (versione 14).
3. Risultati e discussione
3.1. Esame della morfologia superficiale
La superficie del film a base di HPMC puro, mostrata in , è liscia e omogenea, senza la presenza di difetti superficiali o rugosità. Quando la rutina è stata aggiunta a questo film, è stata osservata la presenza di piccole formazioni, probabilmente dovute alla scarsa solubilità della rutina in acqua ( ). Studi precedenti hanno dimostrato che si dissolve bene in etanolo o in mezzi ricchi di etanolo [ 21 ]. Pertanto, per la preparazione della presente serie di film, è stata selezionata una miscela etanolo-acqua con una predominanza di etanolo, in modo che questa miscela fornisca un'adeguata solubilità per ciascuno dei componenti dei film compositi. Risulta che, sebbene la quantità di acqua nel mezzo di dissoluzione sia relativamente bassa (solo il 30%), parte della rutina rimane disciolta o distribuita in modo insufficientemente omogeneo nel volume del film di HPMC, che è la ragione della migrazione parziale in superficie e del cambiamento nella morfologia di questo film. Per migliorare le proprietà superficiali e di barriera del film a base di HPMC puro, sono stati sviluppati anche film in cui la zeina è stata aggiunta in quantità di massa diverse rispetto all'HPMC. Con un rapporto di 3:1 a favore dell'HPMC, si osserva la formazione di depressioni ovali, di dimensioni relativamente uniformi e distribuite uniformemente su tutta la superficie, come si vede dalla c. Quando si aggiunge rutina a questo film modello, si osserva la comparsa di piccoli pori con un diametro medio di circa 1-1,2 µm ( d). Figura 1. Micrografie al microscopio elettronico a scansione di campioni basati su HPMC ( a ), HPMC con rutina ( b ), HPMC 3:1 zeina ( c ), HPMC 3:1 zeina + rutina ( d ), HPMC 1:1 zeina ( e ) e HPMC 1:1 zeina + rutina ( f ).
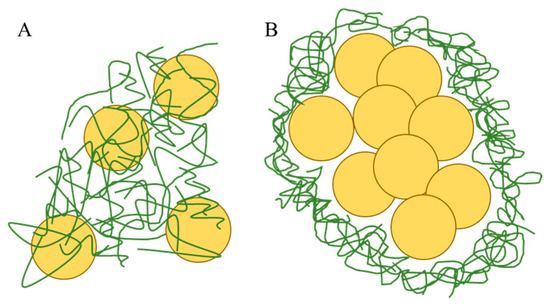
Ciò può essere dovuto a due fattori: l'uso di un plastificante idrosolubile nella preparazione dei film (PEG 400), che forma pori nella matrice di zeina, come riportato da Giteru et al. 2019 [ 22 ], o il fatto che zeina e HPMC hanno diversa solubilità e affinità per diversi tipi di solventi. La zeina è un polimero idrofobico, incline ad aggregarsi e formare particelle in presenza di acqua, e inoltre, quando utilizzata in combinazione con un polimero idrosolubile, si osservano vuoti, come si vede nelle immagini attuali e da altri ricercatori [ 23 ]. Questo comportamento della zeina è confermato e manifestato nella preparazione di un film composito basato su rapporti di massa uguali tra essa e HPMC. Nella micrografia in e, si osserva che oltre alla presenza di depressioni sferiche, si osserva la formazione di particelle sferiche e ovali con un diametro medio di circa 3,30 µm. Poiché la quantità secca utilizzata per preparare i film è sempre la stessa, quando la quantità di zeina aumenta, quella di HPMC diminuisce. Pertanto, si osserva un processo di separazione di fase dovuto alla ridotta viscosità della soluzione totale e all'aumento dell'idrofobicità. Di conseguenza, la formazione di particelle di zeina e la presenza di difetti superficiali sono osservate più chiaramente [ 14 ]. L'inclusione di rutina in questo tipo di film porta nuovamente a un cambiamento evidente nella morfologia superficiale, mostrato in f. Alcune delle particelle di zeina sono visibili sullo strato superiore di questo film, ma oltre a esse, vi è la presenza di rugosità e pieghe significative. Questo tipo di cambiamento nella morfologia è caratteristico dei sistemi in cui la disposizione delle catene polimeriche è disturbata da altri elementi strutturali nella matrice, come la rutina [ 24 ]. Secondo alcuni autori, ciò potrebbe essere dovuto alla formazione di legami idrogeno intermolecolari tra i polimeri stessi o tra i polimeri e la sostanza attiva [ 25 , 26 , 27 ] ( ). Figura 2. Esempio di illustrazione della disposizione dei cluster/particelle di zeina (giallo) tra le catene HPMC (verde): ( A ) per un rapporto 3:1, ( B ) per un rapporto 1:1.
3.2. Spettri infrarossi a trasformata di Fourier di composti nativi e strutture ottenute
Per valutare la compatibilità e la presenza di potenziali interazioni tra le sostanze utilizzate per ottenere le presenti strutture, è stata utilizzata la spettroscopia infrarossa a trasformata di Fourier. Gli spettri ottenuti sono presentati nelle , , , e .
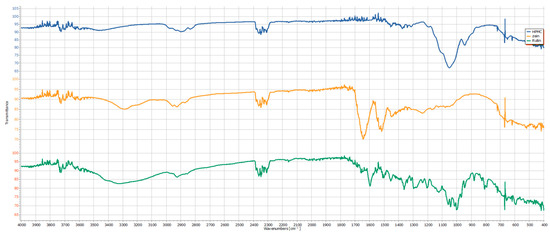
Figura 3. Spettri FTIR di HPMC (linea blu), zeina (linea gialla) e rutina (linea verde).
Figura 4. Spettri FTIR di HPMC (linea blu) e film di HPMC caricato con rutina (linea rossa).
Figura 5. Spettri FTIR di zeina HPMC 3:1 (linea nera), zeina HPMC 3:1 + rutina (linea blu).
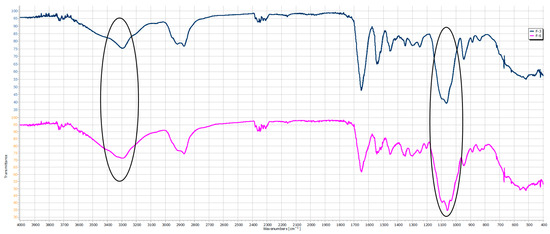
Figura 6. Spettri FTIR di HPMC 1:1 zeina (blu scuro), HPMC 1:1 zeina + rutina (linea magenta).
Figura 7. Energia libera superficiale di tutti i film compositi studiati. Le lettere minuscole nella figura (a–f) indicano differenze nei risultati con un livello di significatività p < 0,05. Tutti i dati presentati nella figura sono statisticamente diversi.
presenta gli spettri di tutti i composti nella loro forma pura. Sulla base di essi, i seguenti numeri di lunghezza d'onda possono essere indicati come picchi caratteristici per HPMC: 3460 cm −1 (gruppi –OH), 2901 cm −1 e 2835 cm −1 (stiramento asimmetrico e simmetrico dei gruppi metilenici nei sostituenti), 1456 cm −1 (piegatura di –CH2 nei gruppi metilici), 1050 cm −1 (vibrazioni di stiramento dei gruppi CO e COC) e 944 cm −1 (associati alle vibrazioni della struttura principale delle macromolecole HPMC e delle regioni amorfe e specificamente alle deformazioni di CO e all'oscillazione di –CH2) [ 28 , 29 , 30 ]. Nello spettro della zeina, si possono riportare le seguenti bande caratteristiche: Zeina—3284 cm −1 (allungamento di –OH e –NH nei gruppi idrossile e amminico), 2927 cm −1 e 2871 cm −1 (allungamento di –CH nei gruppi –CH3 e –CH2, rispettivamente), 1648 cm −1 (allungamento di C=O nell'ammide primaria), 1544 cm −1 (piegatura di NH e allungamento di CN nell'ammide secondaria) e 1236 cm −1 (vibrazioni complesse nell'ammide terziaria, incluso allungamento di CN e piegatura di NH) [ 31 , 32 , 33 ]. I numeri tipici della lunghezza d'onda per la rutina discussi da altri autori e osservati nello spettro dato sono i seguenti: 3327 cm −1 (ampio picco dovuto ai gruppi –OH nell'alcol e in quelli fenolici), 2926 cm −1 (allungamento del CH nei legami CH aromatici e alifatici), 1657 cm −1 (picco debole dovuto al gruppo carbonilico coniugato nella struttura flavonoide), 1596 cm −1 (anelli benzenici), da 1300 cm −1 a 1000 cm −1 (allungamento del CO e del CC negli anelli aromatici) e 879–720 cm −1 (piegatura del CH nei gruppi aromatici) [ 34 , 35 , 36 ]. Per verificare la presenza di un'interazione tra le sostanze, verranno monitorati i cambiamenti in queste bande caratteristiche, come un cambiamento nella loro intensità, uno spostamento nel valore del numero d'onda, la loro completa scomparsa o la comparsa di nuove. In tutte le strutture polimeriche caricate con rutina ( , e ), si osserva un cambiamento nell'intensità o nella forma dei picchi nell'intervallo 3500–3200 cm −1 , così come 1100–1000 cm −1 , rispetto alla sostanza pura, come mostrato in Secondo vari gruppi di ricerca, quando si formano legami a idrogeno, ci si aspetta un cambiamento nel picco per i gruppi –OH, poiché sarebbero potenzialmente coinvolti, così come le bande che indicano lo stiramento del legame CO, poiché i legami a idrogeno che coinvolgono gruppi idrossilici possono cambiare l'ambiente del legame C–O [ 37 , 38 ]. Le differenze qui descritte rientrano esattamente in questi intervalli per i valori del numero d'onda, il che conferma la presenza della formazione di legami idrogeno tra il polifenolo e la matrice polimerica, indipendentemente dalla sua composizione. Considerando i picchi di HPMC e zeina e confrontandoli con la struttura ottenuta, si notano cambiamenti nelle seguenti regioni: 3500–3300 cm −1 , 1700–1600 cm −1 e 1100–1000 cm −1 . Il cambiamento nel primo picco si esprime in un leggero spostamento delle singole bande caratteristiche dei polimeri stessi, nonché in un significativo allargamento di questo picco. Il cambiamento successivo si verifica nella regione dell'ammina primaria, che indica un cambiamento nella struttura secondaria della proteina, dovuto all'interazione con HPMC. L'interazione con la zeina può causare lievi cambiamenti o variazioni di intensità in quest'ultima regione, riflettendo cambiamenti nell'ambiente della matrice polimerica. Questi cambiamenti sono dovuti alla formazione di legami idrogeno tra le due sostanze. La struttura della cellulosa è ricca di gruppi –OH, che agiscono come donatori, e i gruppi carbonilici C=O della zeina agiscono come accettori. Ciò spiega i cambiamenti nei picchi degli spettri osservati [ 14 , 36 ]. Inoltre, nelle regioni di interesse per il numero d'onda sopra menzionate, si osserva una differenza nell'intensità dei picchi delle strutture finali. Ciò può essere spiegato dal principio di funzionamento del metodo. In presenza di legami idrogeno più intensi, si osservano picchi più ampi e rotondi o addirittura picchi con intensità inferiore. Nella modalità di trasmissione, un picco più superficiale significa un assorbimento più forte a quella frequenza, il che può indicare più molecole che partecipano all'interazione, o cambiamenti di dipolo più forti durante la vibrazione, il che è un'indicazione di un'interazione più intensa [ 39 ]. Ciò si osserva nello spettro del rapporto di massa 3:1, dove il rapporto dei gruppi attivi coinvolti nella formazione di legami a idrogeno, basato sul peso dei polimeri e sul numero dei loro gruppi attivi per grammo, è 2,1:1,4 a favore dei gruppi –OH dell'HPMC, mentre a un rapporto di massa di 1:1, questo rapporto cambia a 1,81:2,9, ma già a favore dei gruppi C=O della zeina. Quando la rutina viene aggiunta al rapporto 3:1, si osserva un ulteriore allargamento del picco nella regione 3500–3200 cm −1 . Sono evidenti anche cambiamenti nei picchi caratteristici della rutina a 1362 cm −1 , 1014 cm −1 e 808 cm −1 , suggerendo un'ulteriore formazione di legami a idrogeno. Nello spettro di un film con rapporto di massa 1:1 prima e dopo l'incorporazione di rutina, si possono osservare gli stessi cambiamenti, ma con un'intensità delle bande più debole. A questo rapporto di massa, rimane una maggiore quantità di accettori liberi nelle catene della zeina, che possono interagire con i gruppi –OH della rutina.
3.3. Proprietà meccaniche e di barriera dei campioni studiati
Nella sono riportati i valori del modulo di Young e di vari parametri al punto di rottura (sollecitazione e deformazione), insieme ai parametri di barriera.
Tabella 1. Valori di vari parametri meccanici e di barriera per i film ottenuti prima e dopo l'incorporazione della rutina.
I valori del modulo di Young per film a base di HPMC puro sono in buon accordo con altri studi per film a base di polimeri puri. È interessante notare che nello studio di Athanasopoulou et al. 2025, utilizzando quantità simili di plastificante ma utilizzando glicerolo, sono stati riportati valori di modulo di Young quasi cinque volte superiori e una deformazione relativa di solo l'8% [ 39 ]. Questo elevato modulo di Young indica una struttura e una disposizione delle macromolecole significativamente più compatte, che porta anche a questi bassi valori di deformazione. Ciò è dovuto alla differenza nei pesi molecolari dei due plastificanti: quello del glicerolo è circa quattro volte inferiore a quello del PEG 400. Pertanto, tali strutture sviluppate secondo la presente metodologia presentano una deformazione relativa 10 volte maggiore, da cui consegue che il PEG 400 ha una migliore compatibilità con l'HPMC e un effetto plastificante. Dopo l'aggiunta di zeina al film puro a base di HPMC in un rapporto di 3:1, si osserva un aumento del valore del modulo di Young, ma entrambi i valori rientrano nello stesso gruppo statistico, rendendo questi valori statisticamente insignificanti. Un'ulteriore aggiunta di zeina fino a raggiungere un rapporto di massa di 1:1, determina una differenza significativa per questo parametro. Questo tipo di comportamento per il modulo di Young di questa quantità è stato riportato anche da altri autori [ 40 ]. La ragione di questa tendenza potrebbe essere la formazione e la presenza di legami idrogeno, che ostacolano la mobilità delle macromolecole tra regioni di diversa elettronegatività nelle catene dei due polimeri. Il fatto che i film siano stati ottenuti da una soluzione comune ricca di etanolo facilita ulteriormente il processo di formazione di questi legami, così come la separazione di fase osservata nelle micrografie SEM [ 14 ]. In presenza di legami idrogeno formati, si ottiene una struttura più densa e compatta, che è anche più rigida. Di conseguenza, l'interazione e la formazione di legami idrogeno si indeboliscono, il processo di separazione delle due fasi viene migliorato e la compattezza della disposizione delle macromolecole dei due polimeri viene ridotta [ 23 ]. Ciò porta a una significativa diminuzione del modulo di Young, come notato anche da un cambiamento nella deformazione relativa e nella morfologia. I valori di sforzo di rottura e deformazione diminuiscono monotonicamente con l'aumento della concentrazione di zeina, a causa della separazione di fase tra i due polimeri con diversa solubilità [ 23 ].]. Le proprietà barriera sono inoltre significativamente influenzate dalla presenza di zeina nella struttura complessiva. A seguito della sua inclusione, si osserva una leggera diminuzione della velocità di trasmissione del vapore acqueo. Questo comportamento è prevedibile, data la natura idrofobica della zeina, poiché il processo di diffusione e passaggio delle molecole d'acqua attraverso il volume del campione viene rallentato. I valori ottenuti per i film polimerici relativi a questo parametro rientrano nello stesso gruppo statistico. L'aggiunta di rutina ai film porta a un aumento dei valori del modulo di Young per tutti i campioni compreso tra il 18% e l'85%, e tutti appartengono a gruppi statisticamente significativi. Lo stesso vale per gli altri due parametri, ovvero sforzo e deformazione a rottura. La variazione è più debole per il film di HPMC puro, mentre la variazione maggiore si verifica nel film con rapporti di massa uguali. È probabile che con un rapporto 1:1 ci siano accettori di legami idrogeno liberi nelle catene di zeina che interagiscono con le molecole di rutina, anch'esse ricche di gruppi –OH; Pertanto, si osserva la variazione maggiore nella durezza del film. Per quanto riguarda le proprietà barriera, si osserva un'ulteriore diminuzione della velocità di trasmissione del vapore acqueo con l'aggiunta di rutina. Oltre alla sua scarsa solubilità in acqua, l'inclusione di rutina rallenta ulteriormente il processo di migrazione e passaggio delle molecole d'acqua attraverso il volume dei film. Anche in questo caso, i valori della velocità di trasmissione del vapore acqueo non sono statisticamente diversi. 3.4. Misurazioni della bagnabilità e dell'angolo di contatto
L'idrofobicità superficiale di film di HPMC puro, film di zeina HPMC 1:1, film di zeina HPMC 1:1 con rutina inclusa, film di zeina HPMC 3:1 e film di zeina HPMC 3:1 con rutina inclusa è stata misurata utilizzando il metodo dell'angolo di contatto statico con l'acqua. Seguendo la teoria di Owens e Wendt, è stata calcolata l'energia libera superficiale totale di tutti i film compositi studiati. I risultati ottenuti sono presentati in .
La zeina è una proteina idrofobica, mentre l'HPMC è un polisaccaride idrofilo. Combinandoli, creiamo un materiale con proprietà superficiali bilanciate o modificate a seconda del loro rapporto e della loro interazione. I risultati presentati in mostrano che l'introduzione di una zeina nella matrice HPMC porta a una diminuzione dell'energia libera superficiale e promuove l'idrofobicità. Risultati analoghi per film di HPMC puri sono ottenuti in [ 40 , 41 ]. D'altra parte, i dati mostrati in dimostrano che l'inclusione del polifenolo rutina determina un aumento dell'energia libera superficiale dei campioni testati. L'introduzione di rutina nella struttura provoca un aumento dell'energia libera superficiale da 53,29 ± 0,58 mJ/m 2 (misurata in film HPMC puri) a 55,04 ± 0,24 mJ/m 2 in film HPMC con rutina, da 41,87 ± 0,84 mJ/m 2 (misurata in film HPMC 1:1 zein) a 58,13 ± 1,10 mJ/m 2 in film HPMC 1:1 zein con rutina e da 50,73 ± 0,46 mJ/m 2 (misurata in film HPMC 3:1 zein) a 60,19 ± 1,64 mJ/m 2 in film HPMC 3:1 zein con rutina. Questi valori indicano che l'idrofilia dei compositi aumenta con l'aggiunta del polifenolo rutina nella loro struttura. Ciò potrebbe essere causato dai gruppi polifenolici idrofili, che possono aumentare le interazioni tra la superficie della pellicola e l'acqua, determinando l'aumento dell'energia libera superficiale e la diminuzione dell'angolo di contatto osservati.
Le proprietà idrofile dei film possono anche essere influenzate dalle molecole di zeina presenti nei film. Uno studio di Yang et al. [ 42 ] ha dimostrato che la zeina è relativamente idrofobica a causa dell'elevata concentrazione di amminoacidi idrofobici nella sua struttura. Sebbene la zeina sia considerata una proteina insolubile in acqua, presenta un angolo di contatto inferiore a 90°, che può essere causato dal fatto che la zeina contiene ancora una porzione di amminoacidi idrofili come l'acido glutammico. Ciò potrebbe essere il risultato dell'interruzione della creazione di legami idrogeno nella catena molecolare della zeina, che si tradurrebbe in un aumento del numero di gruppi idrossilici o amminici liberi presenti nella matrice di zeina. Nel loro articolo, Xu et al. [ 43 ] dimostrano che il contenuto di idrogeno dei campioni contenenti solo zeina è il più elevato e diminuisce con l'aggiunta di polifenoli ai film, il che può portare a una maggiore idrofilia della loro superficie. Il contenuto di idrogeno della proteina è determinato dal numero e dalla posizione dei gruppi non polari nella catena molecolare, e qualsiasi introduzione di gruppi idrossilici più idrofili da parte dei polifenoli incorporati può portare a una diminuzione del contenuto complessivo di idrogeno. Un'altra causa di tale diminuzione potrebbe essere l'introduzione di polarità attorno ai residui di tirosina. In combinazione con i polifenoli, i siti idrofobici della zeina hanno influenzato i modelli di ripiegamento della proteina, nascondendo così i gruppi idrofobici eterociclici aromatici nei residui di tirosina della zeina, il che ha causato l'aumento dell'idrofilia dei film polifenolo-zeina studiati. 3.5. Stato di fase e comportamento termico
La stabilità termica e lo stato di fase delle sostanze utilizzate nel presente studio sono mostrati nella e .
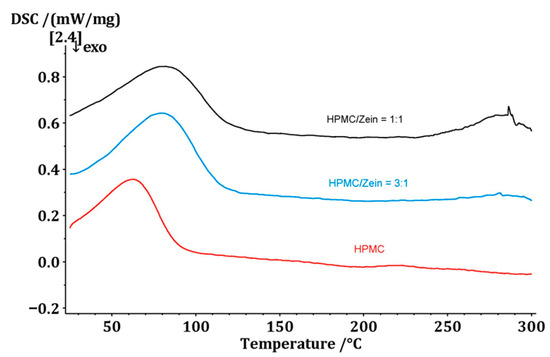
Figura 8. Termogrammi di pellicole basate su HPMC puro, zeina HPMC 3:1 e zeina HPMC 1:1.
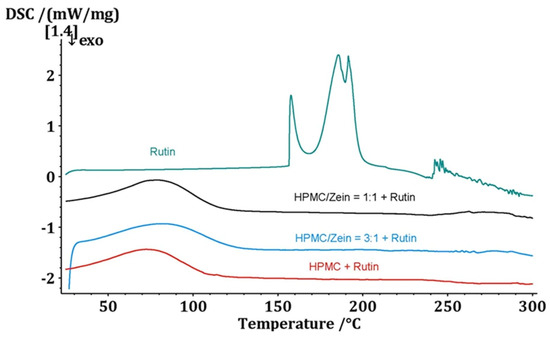
Figura 9. Termogrammi di pellicole a base di rutina pura e di tutte le pellicole con aggiunta di rutina.
Nei termogrammi dei film puri, si osserva un ampio picco, che inizia intorno ai 50 °C e termina intorno o poco dopo i 100 °C. È associato all'evaporazione delle molecole d'acqua non legate [ 15 ]. Una transizione vetrosa dell'HPMC si osserva solitamente intorno ai 160-170 °C, che può essere espressa molto debolmente a seconda della massa del campione [ 44 ]. Per la zeina, sono state riportate temperature di transizione vetrosa comprese tra 94 °C e 98 °C, a seconda delle condizioni di preparazione del film e del grado di aggregazione delle particelle [ 45 ]. A causa della presenza di polimero idrofilo e acqua residua non legata nelle strutture, la regione di temperatura di evaporazione e questa transizione per la zeina si sovrappongono e non possono essere spiegate. Un ulteriore picco endotermico si osserva intorno ai 280 °C, associato alla distruzione termica della zeina. L'area sotto questo picco è proporzionale alla quantità di zeina nella struttura complessiva [ 15 ]. Per la rutina pura, si possono osservare eventi termici a circa 160 °C, due picchi adiacenti tra 185 °C e 200 °C e un altro piccolo picco endotermico dopo 250 °C. Il primo picco è associato alla transizione dallo stato solido a quello liquido del principio attivo, noto anche come fusione. I successivi picchi doppi sono un'indicazione di degradazione termica o, nel caso di quest'ultimo, di decostruzione della rutina [ 46 ]. 3.6. Attività antiossidante contro la soluzione di radicali liberi DPPH
Nella sono mostrati i valori dell'attività antiossidante dei film caricati con rutina (grafico a barre) e la variazione del modulo di Young (grafico lineare).
Figura 10. Modulo di Young e attività di scavenging di pellicole a cui è stata aggiunta rutina.
Il motivo per cui questi risultati vengono presentati insieme è che esiste una tendenza ricorrente nei loro valori e la variazione nei valori di questi parametri è dovuta alla stessa causa principale, ovvero i legami idrogeno. La presenza di tali legami e l'interazione tra la matrice e il polifenolo attraverso di essi portano a un aumento della sua stabilità, nonché a un miglioramento della sua attività inibitoria contro i radicali attivi [ 47 ]. Tutti i campioni mostrano una capacità di rimozione dei radicali ossidativi superiore al 90%, con il valore più alto osservato per il campione 3:1, a favore dell'HPMC. Questo campione presenta anche il valore più alto del modulo di Young. Come precedentemente indicato, dai rapporti studiati finora, si osserva una compatibilità ottimale e la formazione di film tra i due polimeri con un rapporto di massa di 3:1. I film con forti legami idrogeno e una struttura compatta mostrano spesso proprietà antiossidanti migliorate, come osservato nei film HPMC funzionalizzati con zeina e agenti attivi, impedendo la degradazione delle sostanze attive limitando la permeabilità all'ossigeno e all'umidità, aumentando così l'efficacia antiossidante complessiva del film composito [ 48 ]. Al secondo posto in termini di attività antiossidante si trova il film con la presenza di zeina, a causa di reti più estese di legami idrogeno. Allo stesso tempo, l'HPMC stesso può formare tali legami solo con molecole d'acqua, con un'intensità significativamente inferiore. Pertanto, i film basati su HPMC puro hanno una debole attività antiossidante e la loro funzionalizzazione con altri polimeri e sostanze attive è necessaria per ottenere proprietà antiossidanti e potenzialmente di confezionamento ottimali [ 7 , 48 ]. 4. Conclusioni
Questo studio dimostra che i film multicomponenti HPMC-zeina, se arricchiti con rutina, possiedono un forte potenziale come materiali di imballaggio attivi sostenibili. La miscelazione di HPMC con zeina ha portato a una separazione di fase controllata e alla formazione di legami a idrogeno, che hanno influenzato la morfologia, le proprietà meccaniche e le prestazioni barriera dei film. La formulazione HPMC-zeina = 3:1 ha mostrato il comportamento più equilibrato, combinando una maggiore rigidità, una ridotta trasmissione del vapore acqueo e una microstruttura stabile. L'incorporazione di rutina ha ulteriormente migliorato la rigidità del film, modificato l'idrofilia superficiale e aumentato significativamente l'attività antiossidante, con tutti i film caricati con rutina che hanno raggiunto efficienze di scavenging superiori al 90%. Questi miglioramenti derivano dalle forti interazioni tra il polifenolo e la matrice polimerica, che promuovono stabilità e prestazioni funzionali. I risultati indicano che i film HPMC-zeina arricchiti con rutina rappresentano una promettente piattaforma biodegradabile per l'imballaggio alimentare attivo, in particolare per applicazioni in cui sono desiderabili una maggiore rigidità e una protezione antiossidante. Gli studi futuri dovrebbero concentrarsi sulla messa a punto della flessibilità della pellicola e della sensibilità all'umidità per specifiche categorie di alimenti, valutandone le prestazioni in sistemi alimentari reali e ottimizzando il rilascio del composto attivo per garantire l'applicabilità pratica su una gamma più ampia di prodotti.
Contributi degli autori
Concettualizzazione, SM e AV; metodologia, SM, MM e AV; analisi formale, SM, MM e AV; indagine, AV; risorse, AV; cura dei dati, MM; scrittura: preparazione della bozza originale, SM; scrittura: revisione e modifica, MM e AV; visualizzazione, SM; supervisione, SM; amministrazione del progetto, AV; acquisizione dei finanziamenti, AV Tutti gli autori hanno letto e accettato la versione pubblicata del manoscritto.
Finanziamento
Questa ricerca è stata finanziata dal programma NextGenerationEU dell'Unione Europea, attraverso il Piano nazionale di ripresa e resilienza della Repubblica di Bulgaria, progetto DUECOS BG-RRP-2.004-0001-C01, D24-FTF-009.
Dichiarazione del Comitato di revisione istituzionale
Non applicabile.
Dichiarazione di consenso informato
Non applicabile.
Dichiarazione di disponibilità dei dati
I contributi originali presentati in questo studio sono inclusi nell'articolo. Ulteriori informazioni possono essere richieste ai rispettivi autori.
Conflitti di interesse
Gli autori dichiarano di non avere conflitti di interesse.
Riferimenti
- Ahmed, MW; Haque, MA; Mohibbullah, M.; Khan, MSI; Islam, MA; Mondal, MHT; Ahmmed, R. Una revisione degli imballaggi attivi per la qualità e la sicurezza degli alimenti: tendenze attuali, applicazioni, prospettive e sfide. Food Packag. Shelf Life 2022 , 33 , 100913. [ Google Scholar ] [ CrossRef ]
- Vasile, C.; Baican, M. Progressi nel confezionamento alimentare, nella qualità e nella sicurezza alimentare: confezionamento antiossidante e/o antimicrobico a rilascio controllato. Molecules 2021 , 26 , 1263. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Du, H.; Sun, X.; Chong, X.; Yang, M.; Zhu, Z.; Wen, Y. Una revisione sui sistemi di imballaggio attivi intelligenti per la conservazione degli alimenti: applicazioni e tendenze future. Trends Food Sci. Technol. 2023 , 141 , 104200. [ Google Scholar ] [ CrossRef ]
- Narasagoudr, SS; Hegde, VG; Chougale, RB; Masti, SP; Vootla, S.; Malabadi, RB Proprietà fisico-chimiche e funzionali di pellicole bioattive di chitosano/alcol polivinilico indotte dalla rutina per applicazioni di imballaggio alimentare. Food Hydrocoll. 2020 , 109 , 106096. [ Google Scholar ] [ CrossRef ]
- Tang, P.; Li, X.; Li, H.; Li, J.; Tang, B.; Zheng, T. Sviluppo di una pellicola attiva a base di collagene e idrossipropilmetilcellulosa contenente polifenolo di mela per il confezionamento alimentare. Int. J. Biol. Macromol. 2024 , 273 , 132960. [ Google Scholar ] [ CrossRef ]
- Bilbao-Sáinz, C.; Avena-Bustillos, RJ; Wood, DF; Williams, TG; McHugh, TH Film commestibili compositi a base di idrossipropilmetilcellulosa rinforzati con nanoparticelle di cellulosa microcristallina. J. Agric. Food Chem. 2010 , 58 , 3753–3760. [ Google Scholar ] [ CrossRef ]
- Ghadermazi, R.; Hamdipour, S.; Sadeghi, K.; Ghadermazi, R.; Khosrowshahi Asl, A. Effetto di vari additivi sulle proprietà di pellicole e rivestimenti derivati da idrossipropilmetilcellulosa: una revisione. Food Sci. Nutr. 2019 , 7 , 3363–3377. [ Google Scholar ] [ CrossRef ]
- Zheng, M.; Chen, J.; Tan, KB; Chen, M.; Zhu, Y. Sviluppo di una pellicola di idrossipropilmetilcellulosa con gomma xantana e sua applicazione come biomateriale per il confezionamento alimentare nel miglioramento della durata di conservazione delle banane. Food Chem. 2022 , 374 , 131794. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Sun, Y.; Ma, Y.; Hou, Y.; Jia, S.; Cheng, S.; Su, W.; Tan, M.; Zhu, B.; Wang, H. Preparazione di una pellicola intelligente sensibile al pH basata su proteine lipofile di soia/idrossipropilmetilcellulosa per il monitoraggio della freschezza del salmone. Food Packag. Shelf Life 2025 , 47 , 101436. [ Google Scholar ] [ CrossRef ]
- Gillgren, T.; Stading, M. Proprietà meccaniche e di barriera dei film di avenina, kafirina e zeina. Food Biophys. 2008 , 3 , 287–294. [ Google Scholar ] [ CrossRef ]
- Singh, N.; Singh, S.; Kaur, A.; Singh Bakshi, M. Zein: Struttura, produzione, proprietà dei film e applicazioni. In Natural Polymers ; RSC Publishing: Cambridge, Regno Unito, 2012. [ Google Scholar ] [ CrossRef ]
- Bayer, IS Zein nel packaging alimentare. In Sustainable Food Packaging Technology ; Wiley-VCH: Weinheim, Germania, 2021; pp. 199–224. [ Google Scholar ] [ CrossRef ]
- Özçalık, O. Preparazione e caratterizzazione di pellicole in polipropilene rivestite con nanocompositi di zeina di mais per applicazioni di imballaggio alimentare. Tesi di laurea magistrale, Istituto di tecnologia di Izmir, Smirne, Turchia, 2010. [ Google Scholar ]
- Zhang, Y.; Bonilla, J.; Joye, IJ; Lim, LT Proprietà fisico-chimiche di pellicole commestibili formate dalla separazione di fase di zeina e idrossipropilmetilcellulosa. LWT 2025 , 218 , 117504. [ Google Scholar ] [ CrossRef ]
- Ferreira, JO; Zambuzi, Georgia; Camargos, CH; Carvalho, AC; Ferreira, deputato; Rezende, California; de Freitas, O.; Francisco, KR Zein e microfibre di acetato succinato di idrossipropilmetilcellulosa per il trattamento parodontale. interno J. Biol. Macromol. 2024 , 261 , 129701. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Sharma, S.; Mulrey, L.; Byrne, M.; Jaiswal, AK; Jaiswal, S. Incapsulamento di oli essenziali in nanovettori per imballaggi alimentari attivi. Foods 2022 , 11 , 2337. [ Google Scholar ] [ CrossRef ]
- Ge, S.; Li, Q.; Jia, R.; Liu, W.; Liu, M.; Liu, H.; Zheng, M.; Cai, D.; Liu, J. Nanoparticelle composite di zeina/acido gallico per migliorare la stabilità all'ossidazione dell'emulsione Pickering di olio di mais. Food Sci. 2022 , 43 , 78–85. [ Google Scholar ] [ CrossRef ]
- Du, J.; Zhu, Q.; Guo, J.; Gu, J.; Guo, J.; Wu, Y.; Ren, L.; Yang, S.; Jiang, J. Preparazione e caratterizzazione di pellicole commestibili da gelatina e HPMC/CMC. Heliyon 2025 , 11 , e41613. [ Google Scholar ] [ CrossRef ]
- Wang, Y.; Padua, GW Formazione di microfasi di zeina in etanolo-acqua. Langmuir 2010 , 26 , 12897–12901. [ Google Scholar ] [ CrossRef ]
- Owens, DK; Wendt, RC Stima dell'energia libera superficiale del polimero. J. Appl. Polym. Sci. 1969 , 13 , 1741–1747. [ Google Scholar ] [ CrossRef ]
- Krewson, CF; Naghski, J. Alcune proprietà fisiche della rutina. J. Am. Pharm. Assoc. 1952 , 41 , 582–587. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Giteru, SG; Ali, MA; Oey, I. Forza del solvente ed effetti della miscelazione dei biopolimeri su film di zeina-chitosano-PVA. Food Hydrocoll. 2019 , 87 , 270–286. [ Google Scholar ] [ CrossRef ]
- Tian, Y.; Yang, X.; Cao, C.; Lv, Z.; Han, C.; Guo, Q.; Duan, Y.; Zhang, J. Attività antiossidanti migliorate di pellicole commestibili con zeina/polisaccaride contenente curcumina. Food Biosci. 2024 , 57 , 103538. [ Google Scholar ] [ CrossRef ]
- Zhang, S.; Zhao, H. Preparazione e proprietà di film di nanoparticelle composite di zeina-rutina/amido di mais. Carbohydr. Polym. 2017 , 169 , 385–392. [ Google Scholar ] [ CrossRef ]
- Kraisit, P.; Limmatvapirat, S.; Nunthanid, J.; Sriamornsak, P.; Luangtana-Anan, M. Film di miscela mucoadesiva HPMC/policarbofilo tramite progettazione della miscela. Chem. Pharm. Bull. 2017 , 65 , 284–294. [ Google Scholar ] [ CrossRef ]
- Naeem, A.; Yu, C.; Zang, Z.; Zhu, W.; Deng, X.; Guan, Y. Sintesi e valutazione di complessi di inclusione di rutina-idrossipropil β-ciclodestrina incorporati in idrogel a base di gomma di xantano (HPMC- g -AMPS) per la somministrazione orale controllata di farmaci. Antiossidanti 2023 , 12 , 552. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Tivano, F.; Chiono, V. Zein come materiale rinnovabile per nanoparticelle verdi. Front. Biomater. Sci. 2023 , 2 , 1156403. [ Google Scholar ] [ CrossRef ]
- Zaltariov, MF Indagine FTIR sulla cristallinità delle miscele HPMC. Cellul. Chem. Technol. 2021 , 55 , 981–988. [ Google Scholar ] [ CrossRef ]
- Zaltariov, MF; Filip, D.; Varganici, CD; Macocinschi, D. Studi ATR-FTIR e sul comportamento termico di nuove formulazioni di idrogel basate su miscele polimeriche HPMC/PAA. Cellul. Chem. Technol. 2018 , 52 , 619–631. [ Google Scholar ]
- Akinosho, H.; Hawkins, S.; Wicker, L. Analisi dei sostituenti HPMC e reologia. Carbohydr. Polym. 2013 , 98 , 276–281. [ Google Scholar ] [ CrossRef ]
- Karthikeyan, K.; Vijayalakshmi, E.; Korrapati, PS Interazioni delle microsfere di zeina con i farmaci. AAPS PharmSciTech 2014 , 15 , 1172–1180. [ Google Scholar ] [ CrossRef ]
- Dong, S.; Gao, A.; Zhao, Y.; Li, YT; Chen, Y. Proprietà della zeina modificata con plasma freddo. Food Bioprod. Process. 2017 , 106 , 65–74. [ Google Scholar ] [ CrossRef ]
- Liu, G.; An, D.; Li, J.; Deng, S. Nanoparticelle a base di zeina: preparazione, caratterizzazione e applicazione farmaceutica. Front. Pharmacol. 2023 , 14 , 1120251. [ Google Scholar ] [ CrossRef ]
- Immaculate, AA; Vimala, JR; Takuwa, DT Isolamento e caratterizzazione della rutina da Cadaba aphylla e Adenia glauca . Orient. J. Chem. 2022 , 38 , 1404–1412. [ Google Scholar ] [ CrossRef ]
- Paczkowska, M.; Lewandowska, K.; Bednarski, W.; Mizera, M.; Podborska, A.; Krause, A.; Cielecka-Piontek, J. Identificazione spettroscopica della quercetina-3-O-rutinoside. Spettrochim. Atto A 2015 , 140 , 132–139. [ Google Scholar ] [ CrossRef ]
- Nutrizio, M.; Juric, S.; Kucljak, D.; Švaljek, SL; Vlahoviček-Kahlina, K.; Jambrak, AR; Vinceković, M. Incapsulamento di estratti di rosmarino in microparticelle di alginato/zeina/HPMC. Alimenti 2023 , 12 , 1570.
- Madkour, DA; Ahmed, M.; Elkirdasy, AF; Orabi, SH; Mousa, AA Rutina: proprietà chimiche e biologiche. Matrouh J. Vet. Med. 2024 , 4 , 26–34. [ Google Scholar ] [ CrossRef ]
- Krysa, M.; Szymańska-Chargot, M.; Zdunek, A. Impronte digitali FT-IR e FT-Raman dei flavonoidi. Food Chem. 2022 , 393 , 133430. [ Google Scholar ] [ CrossRef ]
- Athanasopoulou, E.; Maurizzi, E.; Bigi, F.; Quartieri, A.; Pulvirenti, A.; Tsironi, T. Effetto comparativo di diversi plastificanti sulle proprietà fisico-chimiche di film a base di idrossipropilmetilcellulosa (HPMC) adatti al confezionamento dell'orata. Carbohydr. Polym. Technol. Appl. 2025 , 10 , 100839. [ Google Scholar ] [ CrossRef ]
- Gilbert, J.; Cheng, CJ; Jones, OG Barriera al vapore e proprietà meccaniche dei film di nanoparticelle HPMC/zeina. Food Biophys. 2018 , 13 , 25–36. [ Google Scholar ] [ CrossRef ]
- Luner, PE; Oh, E. Caratterizzazione dell'energia libera superficiale dei film di etere di cellulosa. Colloids Surf. A 2001 , 181 , 31–48. [ Google Scholar ] [ CrossRef ]
- Yang, J.; Xie, J.; Paximada, E. Particelle di zeina/quercetina elettrospruzzate: formazione e proprietà. Bioprocesso alimentare. Technol. 2025 , 18 , 2840–2853. [ Google Scholar ] [ CrossRef ]
- Xu, Y.; Wei, Z.; Xue, C.; Huang, Q. Assemblaggio di coniugati zeina-polifenoli. LWT 2022 , 154 , 112708. [ Google Scholar ] [ CrossRef ]
- McPhillips, H.; Craig, DQM; Royall, PG; Hill, VL Transizione vetrosa di HPMC utilizzando MTDSC. Int. J. Pharm. 1999 , 180 , 83–90. [ Google Scholar ] [ CrossRef ]
- Bisharat, L.; Berardi, A.; Perinelli, DR; Bonacucina, G.; Casettari, L.; Cespi, M.; AlKhatib, HS; Palmieri, GF Aggregazione di zeina in dispersioni di etanolo: effetto sulle proprietà del film. interno J. Biol. Macromol. 2018 , 106 , 360–368. [ Google Scholar ] [ CrossRef ]
- Marudova, M.; Viraneva, A.; Milenkova, S.; Shivachev, B.; Titorenkova, R.; Tarassov, M. Miscele polifenoli/PLA: struttura, proprietà termiche ed elettrete. Bulg. Chimica. Comune. 2025 , 57 , 5–10. [ Google Scholar ]
- Gagliardi, A.; Voci, S.; Paolino, D.; Fresta, M.; Cosco, D. Influenza dei composti modello sui gel a base di zeina. Molecules 2020 , 25 , 3174. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Yao, L.; Man, T.; Xiong, X.; Wang, Y.; Duan, X.; Xiong, X. Film HPMC funzionalizzati da emulsioni zeina/CTG. Int. J. Biol. Macromol. 2023 , 238 , 124053. [ Google Scholar ] [ CrossRef ] [ PubMed ]
| Disclaimer/Nota dell'editore: le dichiarazioni, le opinioni e i dati contenuti in tutte le pubblicazioni sono esclusivamente quelli dei singoli autori e collaboratori e non di MDPI e/o del/i curatore/i. MDPI e/o il/i curatore/i declinano ogni responsabilità per eventuali danni a persone o proprietà derivanti da idee, metodi, istruzioni o prodotti a cui si fa riferimento nel contenuto. |






Nessun commento:
Posta un commento